Дек
Вакцины от рака возглавили десятку научных прорывов года
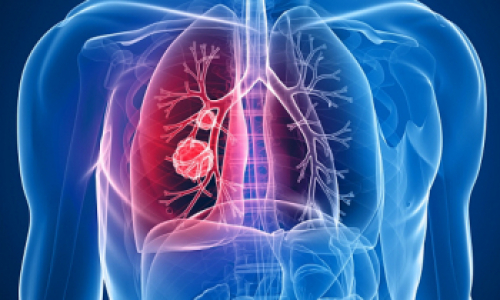
Иммунотерапия онкологических заболеваний возглавила рейтинг наиболее значительных научных достижений 2013 года, составленный журналом Science и опубликованный в его номере от 20 декабря. В топ-10 также вошли еще семь открытий в области медицины, генетики и биологии.
«Этот год безошибочно можно назвать годом иммунотерапии рака за грандиозный и многообещающий прорыв в этой области, — заявил Тим Аппенцеллер (Tim Appenzeller), шеф новостной редакции Science. — Пока терапевтическая стратегия, связанная с активацией иммунного ответа организма на опухолевые клетки, сработала лишь для некоторых видов рака и в отношении узкого круга пациентов, поэтому не стоит ожидать ее скорого широкого применения в клинической практике. Но многие специалисты по онкологическим заболеваниям убеждены, что являются свидетелями рождения принципиально новой парадигмы терапии рака».
Истоки сегодняшнего успеха иммунотерапии раковых заболеваний уходят в 1980-е годы, когда французские исследователи открыли поверхностный рецептор Т-клеток иммунной системы CTLA-4, тормозящий их активность в отношении чужеродных агентов. Позже, в середине 1990-х годов, было доказано на мышах, что блокирование CTLA-4 приводит к разрушению опухолевых клеток Т-клетками иммунной системы. Соответствующее антитело было разработано в конце 1990-х годов, а в 2010 году были опубликованы результаты его первых клинических испытаний, показавшие, что продолжительность жизни пациентов с метастазированной меланомой, получавших такую терапию, увеличилась в среднем на 4 месяца по сравнению с теми, кто ее не получал, пишет medportal.ru.
В начале 1990-х годов японские исследователи нашли еще один молекулярный фактор, оказывающий тормозящее действие на Т-клетки, PD-1. Клинические испытания блокирующего PD-1 антитела на 39 пациентах с пятью различными видами рака начались в 2006 году. Спустя два года у пяти участников с резистентным к стандартной терапии раком опухоли значительно уменьшились, а уровень выживаемости участников в целом оказался намного выше, чем прогнозировалось. В 2012 году стали известны результаты испытаний анти-PD-1-терапии на почти 300 пациентах с различными видами рака. Значительное уменьшение объема опухолей было зафиксировано у 31 процента участников с меланомой, у 29 процентов – с раком почки, и в 17 процентах случаев рака легких.
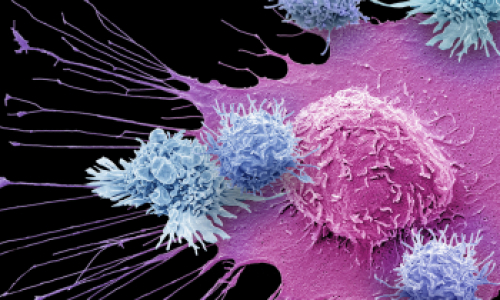
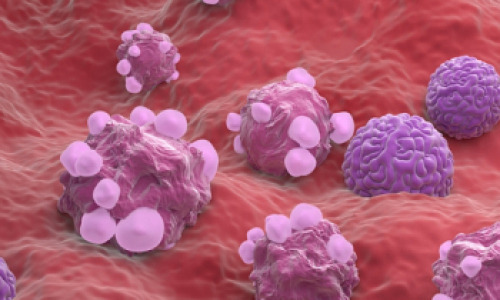
Иллюстрация с сайта sciencemag.org, демонстрирующая работу антител (розовый), блокирующих рецептор на поверхности Т-клетки (лиловый), что запускает цепную реакцию, результатом которой становится атака иммунной системы на клетки опухоли.
К настоящему времени методами терапии рака на основе антител заинтересовались крупнейшие фармкомпании мира. По крайне мере пять фармгигантов уже разработали блокирующие PD-1 и CTLA-4 экспериментальные препараты. Так, в 2011 году Управление по продуктам и лекарствам США (FDA) одобрило разработку Bristol-Myers Squibb Yervoy (ipilimumab), представляющую собой CTLA-4-антитело, для терапии метастазированной меланомы. В конце 2013 года компания сообщила, что среди 1800 пациентов, получающих лечение этим препаратом, у 22 процентов продолжительность жизни достигла трех лет после постановки диагноза. Кроме того, в июне стало известно о значительном усилении терапевтического эффекта в результате комбинации ipilimumab’а и анти-PD-1-препарата, приведшей к «глубокой и быстрой регрессии опухоли» у трети пациентов с меланомой. Блокирующие PD-1 антитела пока не получили разрешения к клиническому применению, но, как ожидают эксперты, вскоре это должно случиться.
В 2010 году были опубликованы результаты успешных клинических испытаний еще одного направления иммунотерапии рака – так называемой CAR-терапии (chimericantigen receptor therapy). Этот метод персонализированной терапии подразумевает направленную генетическую модификацию Т-клеток пациента, с тем, чтобы мишенями последних становились исключительно опухолевые клетки. CAR-терапия сейчас находится в фокусе многочисленных клинических испытаний. Только в декабре 2013 года две группы исследователей, из Пенсильванского университета и Memorial Sloan-Kettering Cancer Center (Нью-Йорк) сообщили, что благодаря применению CAR-терапии удалось добиться полной ремиссии у 45 из 75 пациентов с лейкемией, правда у некоторых из них впоследствии наблюдалось обострение заболевания.
Как отмечают в Science, пока остаются не проясненными множество вопросов, связанных с иммунотерапией рака, остающейся все еще экспериментальным методом лечения, в том числе почему она помогает далеко не всем пациентам и не при всех видах раковых заболеваний. В настоящее время ученые заняты поисками биомаркеров, могущих помочь ответить на эти вопросы, а также путей усиления эффективности этого вида терапии.
В топ-10 научных достижений 2013 года также вошли:
— технология редактирования генов CRISPR, основанная на бактериальном белке Cas9, с помощью которого бактерии защищаются от вирусов, «разрезая» их ДНК. В 2012 году ученые смогли использовать этот белок в качестве скальпеля для «микрохирургических» операций на генах. В 2013 году более дюжины групп исследователей со всего мира работают с CRISPR, редактируя специфические гены у мышей, крыс, бактерий, дрожжей, нематод, дрозофил, растений, а также в человеческих клетках, с целью выявления функций генов и возможности применения их для терапии заболеваний.
— разработка ключевого ингридиента вакцины от респираторного синцитиального вируса (РСВ), поражающего миллионы младенцев по всему миру. В 2013 году ученым удалось выделить антитело, вырабатываемое организмом в ответ на РСВ, проанализировать его структуру и создать его синтетический аналог — иммуноген, который станет основой для вакцины.
— новая техника получения изображений структур головного мозга CLARITY, позволившая преодолеть основную проблему существующих методов – непрозрачность тканей из-за липидных молекул, рассеивающих свет в клеточных мембранах. Замена липидов прозрачным гелем позволила сделать ткани транспарентными, оставив видимыми и доступными к изучению нервные клетки и другие структуры мозга.
— значительный прогресс в области выращивания в лабораторных условиях человеческих «мини-органов» из индуцированных плюрипотентных стволовых клеток – зачатков печени, почек и даже рудиментарного головного мозга, что уже позволило, ввиду аналогичности его тканей и структур нормальному мозгу человека, продвинуться в понимании причин микроцефалии.
— выделение стволовых клеток из клонированных человеческих эмбрионов. Добиться такого результата впервые удалось благодаря пониманию роли в этом процессе кофеина, играющего стабилизирующую роль в отношении ключевой молекулы в человеческой яйцеклетке.
— первое научное объяснение необходимости состояния сна для головного мозга. Как оказалось, сон играет ключевую роль в поддержании метаболического гомеостаза — во время сна ткани мозга самоочищаются от токсичных побочных продуктов нейральной активности, накопившихся во время бодрствования.
— выявление определяющего влияния кишечной микрофлоры на практически все процессы, происходящие в организме человека, включая мозговую деятельность, и ее роль в развитии различных заболеваний.